Pile à combustible
|
Descriptif
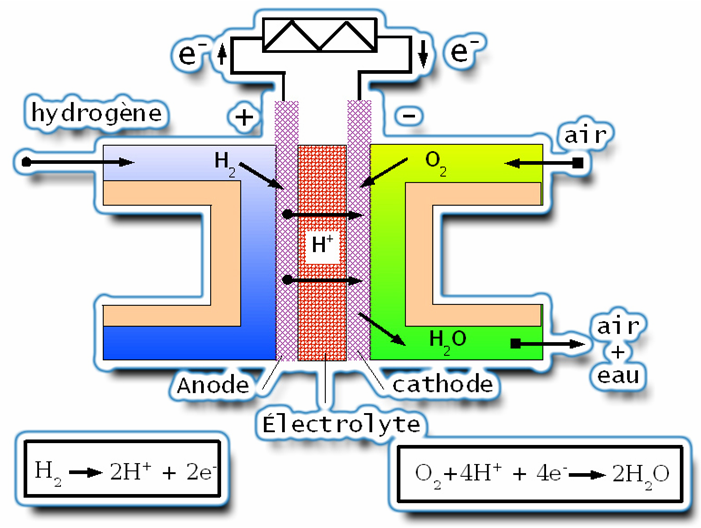
La Cellule a combustible à électrolyte primaire est un dispositif électrochimique constitué par 2 électrodes (anode et cathode) qui n'évoluent pas, un électrolyte et des commandes appropriées. Elle est en mesure de transformer l'énergie chimique des réactifs provenant de l’extérieur (Hydrogène, méthanol, etc...) en énergie électrique sans intermédiation du processus de combustion.Objectif pédagogiques
- Aborder la notion de réversibilité
- Définir la puissance électrique et l'énergie obtenue
- Echanges d'énergie dans une réaction chimique
- Notion d'irréversibilité (pertes ohmiques, perte de diffusion etc.)
- Chute d'activation (lié au courant), Equation de Tafel
- Notion d'efficience ou d'efficacité
- Tracé de la courbe caractéristique de la cellule à combustible dans les conditions « Dead-End » et de la courbe caractéristique de puissance
- Evaluation du rendement de la pile à combustible
Public concerné
Master 1ère annéePré-requis
Thermodynamique, ElectricitéSpécifications techniques
Exemple de résultats

Courbe caractéristique de puissance de la pile
Informations pratiques
| Durée du TP | 3 à 4 heures |
| Nombres d'étudiants minimum/maximum | 2/5 |
| Nombre de dispositif expérimentaux | 1 |
| Notation des étudiants | QCM ou compte-rendu |
| Temps consacré à l'encadrement (% de la durée totale du TP) | ~ ?% |









